Tóm tắt
Trong thập kỷ qua, sản khoa đã tiến một bước dài từ việc chẩn đoán các dị tật bẩm sinh sang sàng lọc và dự báo các biến chứng thai kỳ (như NIPT mở rộng và dự báo tiền sản giật). Giai đoạn 2025-2026 đánh dấu sự khởi đầu của một kỷ nguyên mới thậm chí còn tham vọng hơn: Liệu pháp gen trong bào thai (In utero gene therapy). Bài viết này tổng hợp các cơ chế cốt lõi, các hình thức thử nghiệm lâm sàng hiện hành và những thách thức to lớn nhưng đầy hy vọng của phương pháp điều trị “một lần duy nhất” này, nhằm can thiệp trực tiếp vào mã di truyền của thai nhi để chữa khỏi các bệnh lý di truyền nghiêm trọng ngay trước khi sinh.
1. Cơ chế cốt lõi: lợi dụng “giai đoạn vàng” của bào thai
Liệu pháp gen truyền thống thường gặp khó khăn do hệ miễn dịch của người trưởng thành nhận diện và tấn công các vec-tơ virus dùng để đưa gen lành vào cơ thể. Bào thai, ngược lại, sở hữu một “giai đoạn vàng” đặc biệt.
Cơ chế hành động:
- Hệ miễn dịch chưa hoàn thiện: Ở giai đoạn sớm của thai kỳ (tam cá nguyệt I và II), hệ miễn dịch của thai nhi vẫn đang trong quá trình phát triển và có tính dung nạp miễn dịch (immune tolerance) rất cao. Nếu một gen lành được đưa vào cơ thể thai nhi trong giai đoạn này, hệ miễn dịch có khả năng nhận diện nó là “của mình” thay vì là vật thể lạ, từ đó tránh được phản ứng đào thải sau sinh.
- Tốc độ phân chia tế bào nhanh: Bào thai đang trải qua quá trình phân chia tế bào cực nhanh. Việc đưa gen lành vào các tế bào gốc tạo máu hoặc tế bào đích ở giai đoạn này có thể dẫn đến sự “nhân lên” và phân bố gen lành trên diện rộng đến các cơ quan quan trọng một cách hiệu quả hơn nhiều so với người lớn.
Quy trình điều trị:
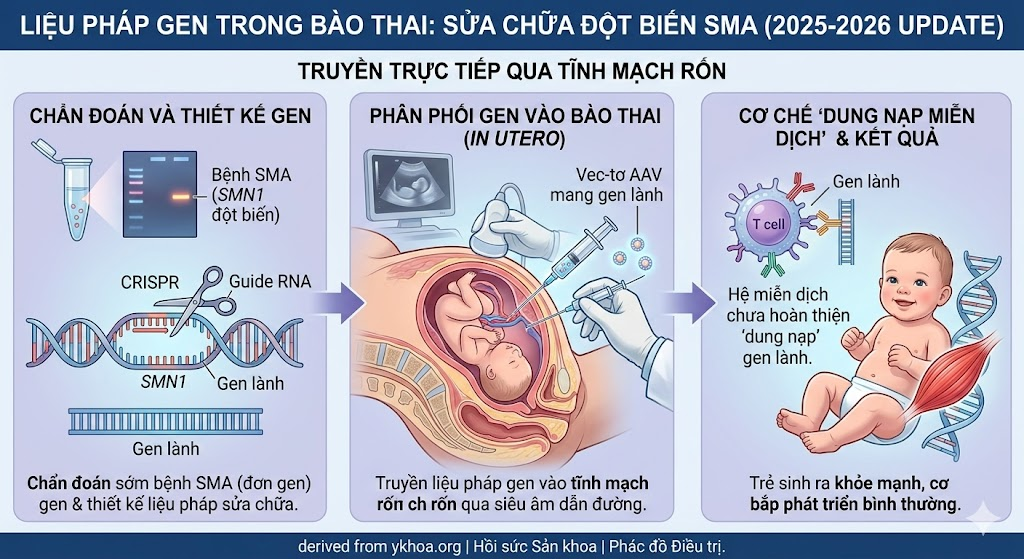
- Chẩn đoán: Bệnh di truyền nghiêm trọng được xác định sớm thông qua NIPT mở rộng hoặc chọc ối.
- Thiết kế gen: Gen lành (hoặc công cụ chỉnh sửa gen như CRISPR-Cas9) được đóng gói vào các vec-tơ vận chuyển (thường là AAV – adeno-associated virus).
- Phân phối gen: Vec-tơ gen được truyền trực tiếp vào bào thai, thường thông qua đường tĩnh mạch rốn (cordocentesis) dưới sự hướng dẫn của siêu âm, tương tự như quy trình truyền máu bào thai.
2. Các hình thức thử nghiệm lâm sàng hiện nay
Giai đoạn 2025-2026 đang chứng kiến những thử nghiệm lâm sàng đầu tiên trên thế giới cho một số bệnh lý di truyền nghiêm trọng.
2.1. Teo cơ tủy (Spinal Muscular Atrophy – SMA)
SMA là bệnh lý thần kinh cơ di truyền lặn nghiêm trọng do đột biến gen SMN1, dẫn đến suy yếu cơ và tử vong sớm.
- Thử nghiệm: Các nghiên cứu đầu tiên đang sử dụng vec-tơ AAV để đưa gen SMN1 lành vào bào thai thông qua tĩnh mạch rốn. Mục tiêu là phục hồi mức protein SMN khỏe mạnh trước khi sự thoái hóa nơ-ron vận động không thể đảo ngược bắt đầu. Dữ liệu ban đầu cho thấy khả năng dung nạp tốt và sự gia tăng nồng độ protein SMN ở trẻ sau sinh.
2.2. Hội chứng Suy giảm miễn dịch Nghiêm trọng (SCID)
SCID, hay còn gọi là “bệnh em bé bong bóng”, là một nhóm bệnh di truyền khiến trẻ không có hệ miễn dịch hoạt động, dẫn đến tử vong do nhiễm trùng trong năm đầu đời.
- Thử nghiệm: Tế bào gốc tạo máu đã được biến đổi gen (ex-vivo hoặc in-vivo) đang được truyền lại cho bào thai. Hy vọng là các tế bào gốc được chỉnh sửa sẽ cư trú thành công trong tủy xương và tạo ra một hệ miễn dịch khỏe mạnh ngay từ khi sinh ra.
3. Thách thức lâm sàng: rào cản và rủi ro
Mặc dù đầy hứa hẹn, liệu pháp gen trong bào thai đối mặt với những thách thức to lớn về an toàn và đạo đức.
- Rủi ro cho mẹ: Quy trình phân phối gen (Cordocentesis) là một kỹ thuật xâm lấn, mang lại rủi ro như sảy thai, vỡ ối sớm, nhiễm trùng hoặc chảy máu cho người mẹ.
- Phản ứng miễn dịch: Mặc dù hệ miễn dịch thai nhi dung nạp tốt, nhưng vẫn có khả năng mẹ phản ứng với vec-tơ virus, hoặc chính thai nhi phát triển phản ứng miễn dịch muộn sau sinh.
- An toàn dài hạn: Lo ngại lớn nhất là “hiệu ứng off-target” (gen lành hoặc CRISPR cắt nhầm gen khác), có thể dẫn đến ung thư về sau. Việc theo dõi lâu dài là tối quan trọng.
- Vấn đề đạo đức: Ai sẽ là người đưa ra quyết định? Ranh giới giữa “chữa bệnh” và “thiết kế con người” là rất mong manh. Cần có các khung pháp lý và đạo đức chặt chẽ.
- Chi phí: Giống như các liệu pháp gen khác, chi phí dự kiến sẽ cực kỳ đắt đỏ, tạo ra thách thức về khả năng tiếp cận.
4. Triển vọng tương lai
Xu hướng trong thập kỷ tới là mở rộng danh sách các bệnh có thể điều trị, bao gồm bệnh tan máu bẩm sinh (Thalassemia), bệnh xương thủy tinh (osteogenesis imperfecta) và các bệnh rối loạn chuyển hóa do thiếu hụt enzyme. Đồng thời, các nhà khoa học đang nghiên cứu các vec-tơ không dùng virus (ví dụ: hạt nano lipid) để tăng cường độ an toàn và giảm nguy cơ off-target.
Tổng kết
Liệu pháp gen trong bào thai là một chương mới đầy hy vọng trong y học thai nhi, mở ra khả năng chữa khỏi hoàn toàn các bệnh lý di truyền nghiêm trọng ngay từ trước khi sinh. Thách thức trong thập kỷ tới là chứng minh tính an toàn dài hạn, xây dựng khung pháp lý đạo đức và đảm bảo khả năng tiếp cận công bằng với liệu pháp tiên tiến này. Đây không còn là khoa học viễn tưởng, mà là một thực tế y khoa đang hình thành.
Tài liệu tham khảo
- June, C. H., et al. (2024). “In utero gene therapy for human genetic diseases: Progress, challenges, and future directions”. Nature Biotechnology.
- Poon, L. C., et al. (The ASPRE Trial Updates). (2025). “The changing landscape of fetal medicine: From screening to in utero therapies”. Ultrasound in Obstetrics & Gynecology.
- National Comprehensive Cancer Network. (2026). Management of immunotherapy-related toxicities (Version 1.2026). https://www.nccn.org
 Y khoa Diễn đàn Y khoa, y tế sức khoẻ, kiến thức lâm sàng, chẩn đoán và điều trị, phác đồ, diễn đàn y khoa, hệ sinh thái y khoa online, mới nhất và đáng tin cậy.
Y khoa Diễn đàn Y khoa, y tế sức khoẻ, kiến thức lâm sàng, chẩn đoán và điều trị, phác đồ, diễn đàn y khoa, hệ sinh thái y khoa online, mới nhất và đáng tin cậy.