Tác giả: Đinh Quang Nhật Ngày: 30/03/2026
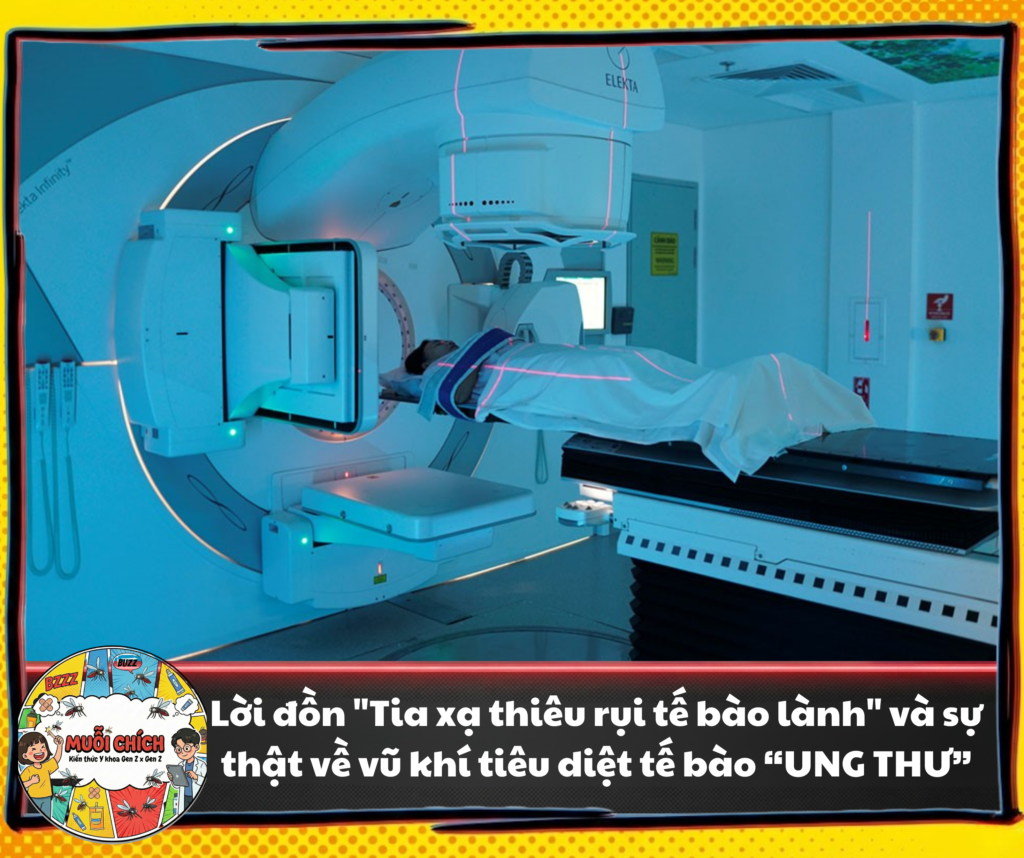
1. Mở đầu: Nỗi ám ảnh mang tên “Thiêu rụi cơ thể” đằng sau cánh cửa phòng xạ trị
Khi nhận được chỉ định xạ trị từ bác sĩ ung bướu, phản ứng đầu tiên của phần lớn bệnh nhân và người nhà thường là sự sợ hãi tột độ. Trong tiềm thức của nhiều người, “tia phóng xạ” đồng nghĩa với chất độc, sự tàn phá và những vết bỏng cháy đen da thịt. Nỗi sợ hãi phổ biến nhất là: “Xạ trị nóng lắm, chiếu tia vào là cháy hết lục phủ ngũ tạng, tế bào ung thư chết thì tế bào lành cũng chết theo, người làm sao mà chịu nổi?” [1].
Tâm lý này hoàn toàn dễ hiểu đối với những người đang mang bệnh nặng. Tuy nhiên, dưới lăng kính của sinh học phân tử và vật lý y khoa hiện đại, việc đánh đồng xạ trị với sự “hủy diệt mù quáng” là một sự hiểu lầm to lớn. Thực chất, tia xạ không hề “ngu ngốc” thiêu rụi mọi thứ trên đường đi của nó. Vậy làm thế nào một chùm tia vô hình lại có thể phân biệt được đâu là khối u cần tiêu diệt, và đâu là mô lành cần được bảo vệ?
2. Hồ sơ khoa học: Cơ chế “Phân biệt Địch – Ta” ở cấp độ ADN
Để hiểu tại sao cơ thể chúng ta không bị “hỏng hết nội tạng” khi xạ trị, chúng ta cần nhìn vào cách các tế bào phản ứng với bức xạ ở cấp độ cấu trúc gen.
2.1. Nghịch lý của sự sinh tồn: Tế bào lành biết “tự chữa lành”
Khi chùm tia bức xạ ion hóa đi qua cơ thể, nó quả thực có gây đứt gãy chuỗi ADN của cả tế bào ung thư lẫn tế bào lành nằm trong trường chiếu [2]. Thế nhưng, điểm khác biệt sống còn nằm ở hệ thống sửa chữa (DNA repair mechanisms). Tế bào khỏe mạnh sở hữu một hệ thống protein sửa chữa ADN cực kỳ tinh vi và hoàn hảo. Ngay khi nhận sát thương, tế bào lành sẽ lập tức tạm dừng chu kỳ phân bào, khởi động cơ chế vá lỗi để khôi phục cấu trúc ADN như ban đầu [3].
2.2. Điểm yếu chí mạng của tế bào ung thư
Ngược lại, đặc tính giúp tế bào ung thư nhân lên điên cuồng cũng chính là gót chân Achilles của chúng: Hệ thống sửa chữa gen của khối u bị khiếm khuyết và đột biến nặng nề (điển hình như đột biến gen p53) [3]. Khi bị tia xạ đánh gãy chuỗi xoắn kép ADN, tế bào ung thư không thể tự “băng bó” vết thương. Cấu trúc di truyền vỡ vụn khiến chúng mất khả năng phân chia và cuối cùng bị ép buộc đi vào con đường chết rụng (Apoptosis) [2]. Nhờ sự chênh lệch về năng lực phục hồi này, mô lành xung quanh vẫn sống sót và tái tạo sau mỗi đợt chiếu tia.
3. Nghệ thuật chia liều (Fractionation): Cho mô lành thời gian “thở”
Nếu bác sĩ dội toàn bộ lượng tia xạ khổng lồ vào cơ thể trong một lần duy nhất, mô lành chắc chắn sẽ bị tổn thương nặng. Tuy nhiên, y học không làm vậy.
Vậy tại sao phải xạ trị mỗi ngày một ít?
Tổng liều bức xạ luôn được bác sĩ chia nhỏ (Fractionation) thành nhiều mũi tiêm (thường từ 20 đến 35 buổi chiếu tia, mỗi ngày một ít, nghỉ cuối tuần) [4]. Việc này dựa trên một tính toán sinh học tuyệt đỉnh: Quãng thời gian 24 giờ giữa 2 buổi xạ trị là vừa đủ để các tế bào lành xung quanh kịp sửa chữa xong các tổn thương ADN và hồi phục hoàn toàn [4]. Trong khi đó, tế bào ung thư sửa chữa chậm chạp nên tổn thương bị cộng dồn ngày qua ngày, cho đến khi chúng gục ngã hoàn toàn.
4. Công nghệ hiện đại: Khi “Bom rải thảm” nhường chỗ cho “Lính tỉa”
Nỗi sợ tia xạ tàn phá mô lành thực chất bắt nguồn từ kỹ thuật xạ trị 2D lạc hậu của vài chục năm trước. Ngày nay, công nghệ xạ trị đã tiến hóa thành nghệ thuật điêu khắc.
4.1. Xạ trị điều biến liều (IMRT) và VMAT
Với công nghệ IMRT, các thiết bị gia tốc tuyến tính có thể xoay 360 độ quanh bệnh nhân, bắn hàng trăm chùm tia nhỏ từ mọi góc độ [5]. Bác sĩ sẽ “nắn” chùm tia bao bọc vừa khít theo hình dáng 3D của khối u. Kết quả là tại tâm khối u (nơi các chùm tia hội tụ), liều bức xạ đạt mức hủy diệt; nhưng ở các mô lành xung quanh, liều lượng chỉ lướt qua cực kỳ mỏng và an toàn [5].
4.2. Chùm tia Proton – Vũ khí không có “đường đạn xuyên thấu”
Đỉnh cao của bảo vệ mô lành là Xạ trị Proton. Khác với tia X thông thường xuyên thẳng qua cơ thể, hạt Proton có đặc tính vật lý độc nhất gọi là “Đỉnh Bragg” (Bragg Peak) [6]. Tia Proton sẽ đi xuyên qua da với năng lượng rất thấp, không gây hại, nhưng khi chạm đúng tọa độ sâu của khối u, nó sẽ bung tỏa toàn bộ năng lượng để phá hủy u, rồi dừng lại ngay lập tức [6]. Các cơ quan nằm ngay phía sau khối u (như tim, tủy sống) sẽ nhận liều bức xạ gần bằng 0, loại bỏ hoàn toàn nguy cơ tổn thương [6].
5. Sự thật về tác dụng phụ: Khu trú chứ không toàn thân
Bệnh nhân thường nghĩ xạ trị sẽ làm rụng tóc, nôn mửa, suy tạng toàn thân. Thực tế, xạ trị là phương pháp điều trị mang tính khu trú (Local treatment) [1]. Nghĩa là, bạn chiếu tia ở đâu thì chỉ vùng đó bị ảnh hưởng. Nếu bạn xạ trị ung thư vú hay ung thư phổi, bạn hoàn toàn không bị rụng tóc trên đầu [1]. Các tác dụng phụ phổ biến nhất như sạm da vùng chiếu (giống như cháy nắng nặng), mệt mỏi hay khô miệng (nếu xạ vùng đầu cổ) đều là các phản ứng viêm tạm thời, và sẽ tự phục hồi sau khi kết thúc liệu trình nhờ khả năng tái tạo của tế bào lành [4].
6. Kết luận
Những tiến bộ vượt bậc của vật lý y khoa và sinh học phân tử đã biến xạ trị từ một “thanh gươm hai lưỡi” thô sơ thành một “bistouri (dao mổ) vô hình” vô cùng sắc bén và chính xác. Tác dụng phụ là có thật, nhưng chúng hoàn toàn nằm trong tầm kiểm soát của bác sĩ và khả năng phục hồi của cơ thể. Đừng để nỗi sợ hãi về những tổn thương “tưởng tượng” khiến bạn đánh mất đi cơ hội vàng để thu hẹp khối u và kéo dài sự sống.
7. Tài liệu tham khảo
- American Cancer Society (ACS). (2024). Radiation Therapy Basics: How Radiation Therapy Works.
- Jackson, S. P., & Bartek, J. (2009). The DNA-damage response in human biology and disease. Nature, 461(7267), 1071-1078.
- Baskar, R., Lee, K. A., Yeo, R., & Yeoh, K. W. (2012). Cancer and radiation therapy: current advances and future directions. International Journal of Medical Sciences, 9(3), 193-199.
- Barton, M. B., et al. (2014). Estimating the demand for radiotherapy from the evidence: a review of changes from 2003 to 2012. Radiotherapy and Oncology, 112(1), 140-144.
- Taylor, A., & Powell, M. E. (2004). Intensity-modulated radiotherapy—what is it?. Cancer Imaging, 4(2), 68.
- Mohan, R., & Grosshans, D. (2017). Proton therapy – present and future. Advanced Drug Delivery Reviews, 109, 26-44.
Cố vấn bài viết: Thạc sĩ – Bác sĩ Hoàng Thị Thuỷ
 Y khoa Diễn đàn Y khoa, y tế sức khoẻ, kiến thức lâm sàng, chẩn đoán và điều trị, phác đồ, diễn đàn y khoa, hệ sinh thái y khoa online, mới nhất và đáng tin cậy.
Y khoa Diễn đàn Y khoa, y tế sức khoẻ, kiến thức lâm sàng, chẩn đoán và điều trị, phác đồ, diễn đàn y khoa, hệ sinh thái y khoa online, mới nhất và đáng tin cậy.