Thế giới y khoa vừa chứng kiến một bước ngoặt lịch sử khi các cơ quan quản lý dược phẩm hàng đầu (như FDA Hoa Kỳ, MHRA Anh Quốc và EMA Châu Âu) lần lượt phê duyệt Casgevy (exagamglogene autotemcel). Đây là phương pháp điều trị đầu tiên trên thế giới sử dụng công nghệ “kéo cắt gen” CRISPR-Cas9 để chữa trị các bệnh lý di truyền. Bài viết này phân tích cơ chế đột phá, dữ liệu lâm sàng mới nhất và những thách thức thực tế khi triển khai liệu pháp trị giá hàng triệu đô la này.
1. Bối cảnh: gánh nặng của bệnh lý huyết sắc tố di truyền
Bệnh Hồng cầu hình liềm (SCD) và Thalassemia thể beta phụ thuộc truyền máu (TDT) là hai bệnh lý di truyền về máu phổ biến và nghiêm trọng. Cả hai đều xuất phát từ đột biến gen sản xuất hemoglobin (huyết sắc tố) – protein vận chuyển oxy trong hồng cầu.
- Bệnh hồng cầu hình liềm: Hồng cầu biến dạng lưỡi liềm, cứng và dính, gây tắc nghẽn mạch máu, dẫn đến các cơn đau cấp tính dữ dội (vaso-occlusive crises – VOCs) và tổn thương đa cơ quan.
- Beta-Thalassemia: Cơ thể không tạo đủ hemoglobin, buộc bệnh nhân phải truyền máu suốt đời, dẫn đến nguy cơ quá tải sắt và các biến chứng tim mạch, nội tiết.
Trước đây, phương pháp chữa khỏi duy nhất là ghép tế bào gốc tủy xương từ người hiến tặng phù hợp – một điều kiện rất khó khăn và đầy rủi ro.
2. Cơ chế đột phá của casgevy: đánh thức “gen ngủ quên”
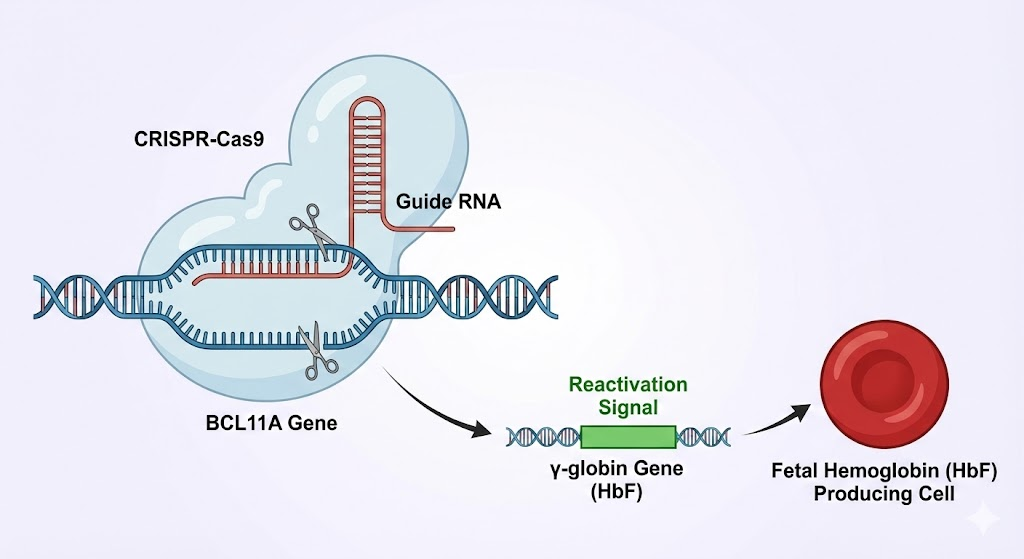
Thay vì cố gắng sửa chữa trực tiếp gen hemoglobin bị lỗi (vốn rất phức tạp), các nhà khoa học đã sử dụng một cách tiếp cận thông minh hơn: Tái kích hoạt Huyết sắc tố bào thai (Fetal Hemoglobin – HbF).
HbF là loại hemoglobin tự nhiên chúng ta có khi còn trong bụng mẹ, có khả năng vận chuyển oxy rất tốt và không bị ảnh hưởng bởi đột biến hình liềm hay thalassemia. Tuy nhiên, sau khi sinh, một gen tên là BCL11A sẽ hoạt động như một chiếc “phanh”, tắt việc sản xuất HbF và chuyển sang sản xuất hemoglobin người lớn (loại bị lỗi ở bệnh nhân).
Quy trình điều trị “một lần duy nhất” (One-time treatment):
- Thu thập: Lấy tế bào gốc tạo máu từ chính bệnh nhân.
- Chỉnh sửa ngoài cơ thể (Ex-vivo): Trong phòng thí nghiệm, công nghệ CRISPR-Cas9 được dùng như một chiếc kéo phân tử, cắt chính xác vào gen BCL11A (chiếc phanh).
- Tái kích hoạt: Khi “phanh” BCL11A bị hỏng, quy trình sản xuất HbF được tái khởi động.
- Truyền lại: Bệnh nhân được điều trị hóa chất (myeloablation) để dọn sạch tủy xương cũ, sau đó truyền lại các tế bào gốc đã được chỉnh sửa. Các tế bào này sẽ sinh sôi và tạo ra hồng cầu mới chứa lượng lớn HbF khỏe mạnh.
3. Dữ liệu lâm sàng cập nhật: hiệu quả bền vững
Các thử nghiệm lâm sàng then chốt (CLIMB-111 và CLIMB-121) và dữ liệu theo dõi dài hạn đến đầu năm 2026 tiếp tục cho thấy những kết quả đáng kinh ngạc:
- Với bệnh Hồng cầu hình liềm: Hơn 95% bệnh nhân tham gia thử nghiệm đã hoàn toàn không còn các cơn đau cấp tính nghiêm trọng (severe VOCs) trong ít nhất 12 tháng liên tục sau điều trị. Chất lượng cuộc sống được cải thiện ngoạn mục.
- Với Beta-Thalassemia: Khoảng 90% bệnh nhân đạt được trạng thái “độc lập truyền máu” (transfusion independence), nghĩa là họ không còn cần truyền máu định kỳ nữa. Số còn lại cũng giảm đáng kể lượng máu cần truyền.
Các dữ liệu mới nhất cho thấy hiệu quả này bền vững theo thời gian, chứng minh rằng các tế bào gốc được chỉnh sửa đã cư trú thành công lâu dài trong tủy xương.
4. Thách thức và tương lai
Dù là một phép màu y học, việc triển khai liệu pháp gen CRISPR đối mặt với những rào cản khổng lồ:
- Chi phí siêu đắt đỏ: Với mức giá niêm yết khoảng 2,2 triệu USD (tại Mỹ) cho một lần điều trị, đây là một trong những loại thuốc đắt nhất thế giới, tạo ra thách thức lớn cho các hệ thống bảo hiểm y tế.
- Quy trình phức tạp và độc hại: Bệnh nhân phải trải qua quá trình hóa trị liệu liều cao để diệt tủy trước khi truyền tế bào, gây ra các tác dụng phụ nghiêm trọng như vô sinh và nguy cơ nhiễm trùng cao trong thời gian nằm viện dài ngày.
- Khả năng tiếp cận: Cần các trung tâm y tế kỹ thuật cao để thực hiện quy trình này. Điều này là rào cản lớn đối với các nước đang phát triển, nơi có gánh nặng bệnh tật cao nhất (như Châu Phi cận Sahara).
- An toàn dài hạn: Dù hiện tại rất an toàn, giới khoa học vẫn cần theo dõi bệnh nhân trong 15 năm tới để đảm bảo không có các “hiệu ứng off-target” (cắt nhầm gen khác) gây ung thư về sau.
KẾT LUẬN
Sự phê duyệt và ứng dụng thành công của liệu pháp CRISPR đầu tiên không chỉ là cứu cánh cho bệnh nhân hồng cầu hình liềm và thalassemia, mà còn là “phát súng hiệu” mở ra kỷ nguyên mới. Hàng loạt nghiên cứu đang được tiến hành để ứng dụng CRISPR trong điều trị ung thư, HIV, và các bệnh di truyền hiếm gặp khác. Chúng ta đang thực sự bước vào thời đại mà con người có thể viết lại mã di truyền của chính mình để chữa bệnh.
Tài liệu tham khảo chính:
- Frangoul, H., et al. (2024). “CRISPR-Cas9 Gene Editing for Sickle Cell Disease and β-Thalassemia”. The New England Journal of Medicine (NEJM).
- FDA News Release (Dec 2023): FDA Approves First Gene Therapies to Treat Patients with Sickle Cell Disease.
- Nature Biotechnology (2025 Review): The clinical progress of CRISPR therapeutics.
 Y khoa Diễn đàn Y khoa, y tế sức khoẻ, kiến thức lâm sàng, chẩn đoán và điều trị, phác đồ, diễn đàn y khoa, hệ sinh thái y khoa online, mới nhất và đáng tin cậy.
Y khoa Diễn đàn Y khoa, y tế sức khoẻ, kiến thức lâm sàng, chẩn đoán và điều trị, phác đồ, diễn đàn y khoa, hệ sinh thái y khoa online, mới nhất và đáng tin cậy.