Carbohydrate (chất đường bột) là nguồn cung cấp năng lượng chính và nhanh chóng cho cơ thể. Quá trình chuyển hóa phức tạp này bao gồm nhiều giai đoạn: tiêu hóa cắt nhỏ đa phân thành đơn phân, vận chuyển qua màng tế bào, và các con đường thoái hóa bên trong tế bào (đường phân, chu trình Krebs) để cấy ghép năng lượng vào phân tử ATP.
I. Tiêu hóa Carbohydrate tại đường ruột
Mục tiêu của quá trình tiêu hóa là cắt đứt các liên kết glycoside để chuyển các phức hợp carbohydrate thành các monosaccharide (đường đơn) để có thể hấp thu được tại ruột non. Diễn biến cụ thể như sau:
- Cắt mảng lớn: Các dạng phức của carbohydrate => Dextrins (chuỗi ngắn, < 8-10 đơn phân).
- Cắt chuỗi ngắn: Dextrins => Disaccharides (đường đôi).
- Cắt đường đôi thành đường đơn: Quá trình này xảy ra tại bờ bàn chải tế bào niêm mạc ruột nhờ các enzyme đặc hiệu:
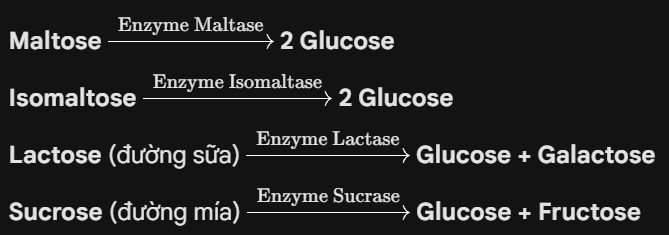
Sản phẩm cuối cùng là các monosaccharide (glucose, fructose, galactose) sẵn sàng được vận chuyển vào máu.
II. Vận chuyển Glucose vào tế bào – Vai trò của Insulin
Sau khi được hấp thu vào máu, glucose cần được vận chuyển qua màng tế bào lipid kép nhờ các protein vận chuyển đặc hiệu gọi là GLUT (Glucose Transporters). Các mô khác nhau bộc lộ các loại GLUT khác nhau, quyết định cách thức mô đó phản ứng với nồng độ đường huyết.
1. Các GLUT quan trọng
- GLUT-1 và GLUT-3: Có ở phần lớn các mô, đặc biệt là não, mô thần kinh, và hồng cầu. Chúng có ái tính rất cao với glucose, đảm bảo vận chuyển mức glucose nền ổn định cho các cơ quan quan trọng này, ngay cả khi cơ thể đang bị hạ đường máu.
- GLUT-2: Có ở tế bào gan và tế bào beta đảo tụy. Chức năng quan trọng bao gồm:
- Tại gan: Có ái tính thấp, thường hoạt động sau bữa ăn (khi đường huyết tăng cao) để vận chuyển phần glucose thừa về gan nhằm mục đích dự trữ (tổng hợp glycogen).
- Tại tụy: Phối hợp cùng enzyme glucokinase, GLUT-2 đóng vai trò như một “cảm biến” nồng độ đường trong máu để kích thích tế bào beta tiết insulin phù hợp.
- GLUT-4: Phổ biến ở mô mỡ và cơ. Đây là loại GLUT đặc biệt vì hoạt động vận chuyển của nó phụ thuộc hoàn toàn vào Insulin.
2. Sự điều hòa của Insulin
Khi nồng độ glucose máu tăng, insulin được tiết ra và kích thích bộc lộ GLUT-4 lên màng tế bào cơ và mô mỡ, làm tăng tốc độ vận chuyển glucose vào các mô này.
- Tại cơ: Glucose thừa được thu nhận và dự trữ dưới dạng glycogen.
- Tại mô mỡ: Glucose được chuyển hóa để tạo dihydroxyacetone phosphate (DHAP) => glycerol phosphate => dùng để ester hóa acid béo tạo triglyceride (mỡ dự trữ).
Note: Glucose làm tăng insulin máu theo 2 cơ chế:
- Giải phóng nhanh các bọc chứa insulin đã được tổng hợp sẵn (xảy ra trong vòng 15 phút).
- Tăng bộc lộ các gen chịu trách nhiệm tổng hợp insulin mới.
III. Con đường đường phân (Glycolysis)
Đường phân là con đường thoái hóa glucose xảy ra trong bào tương của tất cả các tế bào, chuyển một phân tử glucose (6C) thành hai phân tử pyruvate (3C) và tạo ra năng lượng dưới dạng ATP và NADH.
1. Các enzyme và sự điều hòa quan trọng
Phản ứng đường phân có 3 phản ứng một chiều, được xúc tác bởi các enzyme đóng vai trò chủ chốt trong điều hòa:
- Hexokinase (ở mô)/Glucokinase (ở gan): Enzyme đầu tiên “bẫy” glucose vào tế bào bằng cách phosphoryl hóa.
- Phosphofructokinase-1 (PFK-1): Đây là enzyme quan trọng nhất điều hòa tốc độ đường phân.
- Ức chế bởi: ATP (năng lượng cao) và citrate.
- Kích hoạt bởi: AMP (năng lượng thấp).
- Điều hòa nội tiết: Được kích hoạt gián tiếp bởi Insulin và bị ức chế bởi Glucagon thông qua chất trung gian Fructose 2,6-biphosphate (F2,6-BP).
- Insulin => Hoạt hóa PFK-2 => Tạo F2,6-BP => Hoạt hoá mạnh PFK-1 => Tăng đường phân.
- Glucagon => Ức chế PFK-2 => Giảm F2,6-BP => Ức chế PFK-1 => Giảm đường phân.
- Pyruvate kinase: Enzyme cuối cùng tạo ATP. Được kích hoạt bởi Fructose 1,6-biphosphate (cơ chế feed-forward).
Các phản ứng/enzyme khác cần lưu ý:
- Glyceraldehyde 3-phosphate dehydrogenase: Khử NAD+ thành NADH và tạo chất trung gian năng lượng cao 1,3-biphosphoglycerate (1,3-BPG). Trong điều kiện hiếu khí, NADH sẽ được tái oxy hoá ở chuỗi truyền điện tử trong ty thể để tạo ra nhiều ATP hơn.
- 3-phosphoglycerate kinase: Thực hiện phosphoryl hóa mức cơ chất, chuyển nhóm phosphate năng lượng cao từ 1,3-BPG tới ADP để tạo ATP.
2. Các chất trung gian quan trọng
- DHAP: Bên cạnh đường phân, nó còn là nguyên liệu thiết yếu ở gan và mô mỡ để tổng hợp triglyceride.
- 1,3-biphosphoglycerate và phosphoenolpyruvate (PEP): Là các chất trung gian mang năng lượng phosphate cao hơn ATP, được dùng để tổng hợp ATP bằng cơ chế phosphoryl hóa mức cơ chất.
3. Liên hệ sinh lý đặc biệt: Hồng cầu, 2,3-BPG và thích nghi độ cao
Hồng cầu có một nhánh chuyển hóa đặc biệt. Chúng chứa enzyme biphosphoglycerate mutase, xúc tác chuyển chất trung gian 1,3-BPG thành 2,3-biphosphoglycerate (2,3-BPG).
- Vai trò của 2,3-BPG: Chất này gắn vào chuỗi beta của Hemoglobin A (HbA – Hb người lớn) và làm giảm ái tính của Hb đối với oxy. Điều này làm chuyển dịch đường cong phân ly oxy-hemoglobin sang phải, giúp Hb dễ dàng nhường oxy hơn cho các mô.
- Lưu ý: 2,3-BPG gắn không tốt với HbF (Hb thai nhi), đó là lý do HbF có ái tính với oxy cao hơn HbA, giúp lấy oxy từ máu mẹ.
Ứng dụng lâm sàng: Thích nghi với độ cao
Khi lên cao, áp suất oxy giảm, cơ thể sẽ thích nghi qua các giai đoạn:
- Ngay lập tức: Tăng tần số thở => gây kiềm hô hấp => làm giảm P50 (tăng ái tính Hb với oxy) để gắng lấy oxy tại phổi.
- Hóa sinh (12-24h): Tăng tốc độ đường phân => Tăng tổng hợp 2,3-BPG => đưa P50 về mức bình thường (hoặc cao hơn) => giúp nhường oxy cho cơ quan dễ hơn.
- Huyết học (ngày – tuần): Tăng sản xuất Erythropoietin => Tăng hemoglobin và hematocrit.
4. Bệnh lý: Thiếu hụt Pyruvate Kinase
Đây là bệnh lý di truyền gây thiếu máu tan máu bẩm sinh thường gặp thứ 2 (chỉ sau thiếu G6PD).
- Bệnh sinh: Hồng cầu trưởng thành không có ty thể, hoàn toàn phụ thuộc vào ATP từ đường phân để duy trì sự sống. Thiếu ATP làm bơm Na+/K+ ATPase giảm hoạt động => mất cân bằng ion => hồng cầu mất đặc tính lõm 2 mặt và trở nên biến dạng, dễ bị tiêu hủy tại lách (tan máu mạn tính).
- Đặc điểm: Tăng nồng độ 2,3-BPG (do ứ đọng các chất phía trước trong con đường đường phân), gây giảm ái tính của HbA với oxy (giúp bệnh nhân chịu đựng tình trạng thiếu máu tốt hơn). Không có thể Heinz (thể Heinz đặc trưng trong thiếu G6PD).
IV. Chuyển hóa các đường đơn khác (Galactose và Fructose)
1. Chuyển hóa Galactose
Các enzyme quan trọng: Galactokinase và Galactose 1-phosphate uridyltransferase.
Liên hệ lâm sàng: Thiếu hụt enzyme (Galactosemia)
- Ứ đọng galactose gây đặc trưng là đục thủy tinh thể ngay từ khi còn nhỏ. Cơ chế do galactose dư thừa được chuyển hóa bởi aldose reductase tạo thành galactitol – một chất lợi niệu thẩm thấu tích tụ trong thủy tinh thể gây hút nước.
- Thiếu gen galactose 1-phosphate uridyltransferase nghiêm trọng hơn nhiều so với thiếu galactokinase, vì nó gây ứ đọng galactose 1-phosphate (Gal-1-P) – một chất độc đối với tế bào gan, não và các mô.
2. Chuyển hóa Fructose
Các enzyme quan trọng: Fructokinase và Fructose 1-phosphate aldolase (aldolase B).
Liên hệ lâm sàng: Thiếu hụt enzyme
- Thiếu fructokinase (Bệnh Fructose niệu lành tính): Thường không có triệu chứng vì fructose có thể chuyển hóa chậm thông qua enzyme hexokinase của đường phân.
- Thiếu fructose 1-phosphate aldolase (Hội chứng Không dung nạp Fructose di truyền): Rất nghiêm trọng. Ứ đọng Fructose 1-phosphate (F1P) trong tế bào gan và ống lượn gần của thận.
- F1P ứ đọng “bẫy” phosphate hữu cơ trong tế bào, ngăn cản quá trình phosphoryl hóa oxy hóa để tạo ATP, đồng thời ức chế các con đường chuyển hóa carbohydrate khác (glycogenolysis và gluconeogenesis).
- Triệu chứng: Xuất hiện khi trẻ bắt đầu ăn dặm (có sucrose hoặc trái cây), bao gồm: nôn mửa, hạ đường huyết nghiêm trọng sau ăn, gan to, vàng da, và chậm lớn.
V. Phức hệ Pyruvate Dehydrogenase (PDH) – Cầu nối vào ty thể
Sau khi đường phân tạo ra pyruvate trong bào tương, pyruvate được vận chuyển vào ty thể để tiếp tục thoái hóa. Tại đây, nó được chuyển hóa thành Acetyl-CoA nhờ phức hệ Pyruvate Dehydrogenase (PDH).
Các đặc điểm cần nhớ:
- Xảy ra trong ty thể.
- Phản ứng một chiều, không đảo ngược (từ Acetyl-CoA không thể tổng hợp ngược lại pyruvate ở người).
- Điều hòa: PDH ở gan được hoạt hoá bởi insulin (khi năng lượng thừa). PDH ở não và mô thần kinh thì không đáp ứng với hormone, đảm bảo ưu tiên sử dụng pyruvate cho năng lượng.
Phức hệ và các Coenzyme phụ thuộc Vitamin
PDH không phải là một enzyme đơn lẻ mà là một phức hệ đa enzyme rất lớn, cần sự phối hợp của 5 coenzyme khác nhau, có nguồn gốc từ các vitamin nhóm B:
- Thiamine pyrophosphate (TPP): Từ Vitamin B1 (Thiamine).
- FAD(H2): Từ Vitamin B2 (Riboflavin).
- NAD(H): Từ Vitamin B3 (Niacin).
- Coenzyme A (CoA): Từ Acid pantothenic (Vitamin B5).
- Acid lipoic.
VI. Liên hệ lâm sàng
Thiếu hụt Thiamine (Vitamin B1): Thiếu hụt thiamine thường thấy ở những bệnh nhân nghiện rượu kinh niên (do hấp thu kém và dinh dưỡng thiếu sót).
- Bệnh sinh: Khi thiếu thiamine, phức hệ PDH giảm hoạt động. Các mô sử dụng nhiều oxy và năng lượng bị ảnh hưởng đầu tiên: não và cơ tim. Hậu quả là không sản xuất đủ ATP và ứ đọng các ketoacids (như lactate, pyruvate) gây độc.
- Các phức hệ khác cũng cần thiamine và bị ảnh hưởng:
- a-ketoglutarate dehydrogenase (trong chu trình citric/Krebs).
- Phức hệ α-ketoacid dehydrogenase chuỗi nhánh (chuyển hoá các amino acid có nhánh).
- Triệu chứng lâm sàng (Hội chứng Wernicke-Korsakoff và bệnh Beri-beri):
- Thần kinh: Liệt thần kinh vận nhãn, rung giật nhãn cầu (Wernicke); mất trí nhớ và bịa chuyện (Korsakoff); có thể xuất huyết nội sọ.
- Tim mạch: Suy tim sung huyết (bệnh Beri-beri ướt) do cơ tim không đủ ATP để co bóp và bị nhiễm độc ketoacids.
Tài liệu tham khảo
- Victor W. Rodwell, David A. Bender, Kathleen M. Botham, Peter J. Kennelly, P. Anthony Weil. Harper’s Illustrated Biochemistry (32nd ed.). McGraw-Hill Education, 2023.
- Michael Lieberman, Alisa Peet. Marks’ Basic Medical Biochemistry: A Clinical Approach (6th ed.). Wolters Kluwer, 2022.
- John E. Hall, Michael E. Hall. Guyton and Hall Textbook of Medical Physiology (14th ed.). Elsevier, 2021.
- Dennis L. Kasper, Anthony S. Fauci, Stephen L. Hauser, Dan L. Longo, J. Larry Jameson, Joseph Loscalzo. Harrison’s Principles of Internal Medicine (21st ed.). McGraw-Hill Education, 2022.
- Sartori M. “Galactosemia: Clinical features and diagnosis”. UpToDate, 2023.
- Sartori M. “Hereditary fructose intolerance”. UpToDate, 2023.
- Gallagher PG. “Pyruvate kinase deficiency”. UpToDate, 2023.
 Y khoa Diễn đàn Y khoa, y tế sức khoẻ, kiến thức lâm sàng, chẩn đoán và điều trị, phác đồ, diễn đàn y khoa, hệ sinh thái y khoa online, mới nhất và đáng tin cậy.
Y khoa Diễn đàn Y khoa, y tế sức khoẻ, kiến thức lâm sàng, chẩn đoán và điều trị, phác đồ, diễn đàn y khoa, hệ sinh thái y khoa online, mới nhất và đáng tin cậy.