QUY TRÌNH CƠ BẢN ĐỂ PHÁT TRIỂN MỘT VACCINE?
TS. TRẦN BÁ THOẠI
Uỷ viên BCH Hội NỘI TIẾT VIỆT NAM
LỜI MỞ
Theo thống kê của WHO, hiện có hơn ba trăm loại vaccine ngừa COVID-19 đang được thử nghiệm tiền lâm sàng trên động vật và lâm sàng trên người [19] . Ở Việt Nam, công ty Nanogen đang nghiên cứu sản xuất vaccine Nanocovax, với dự kiến sẽ xin sử dụng khẩn cấp vào cuối năm 2022.
Bài viết là tổng quan về quy trình phát triển một vaccine phòng bệnh.
QUY TRÌNH PHÁT TRIỂN VACCINE
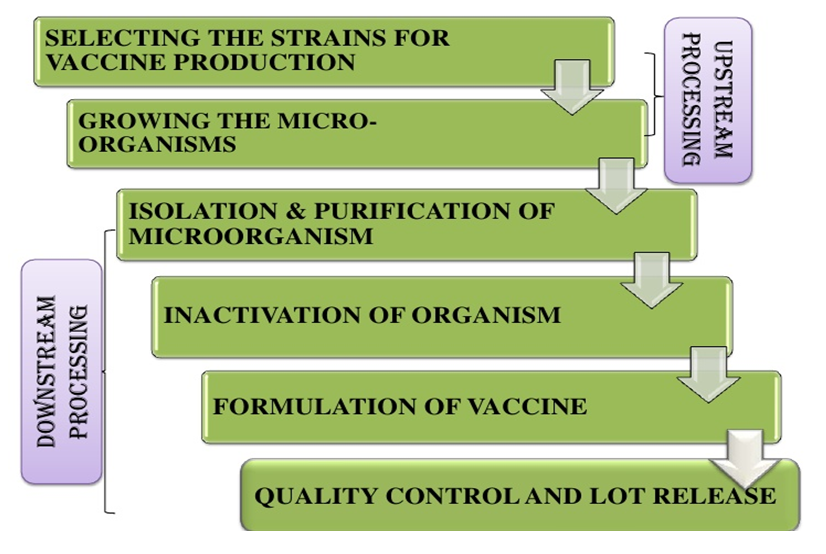
Phát triển một vaccinethường phải đi qua các bước cơ bản sau:
Bước 1 Phân lập và nuôi cấy được virus
Nhờ phân lập và nuôi cấy được virus gây bệnh, các nhà khoa học mới tìm hiểu được cấu trúc, các nhân lên, đặc biệt là biết được yếu tố, protein có tính kháng nguyên… Đây là bước đầu cơ bản để thiết kế một kế hoạch khoa học cho cả quy trình sản xuất, bắt đầu từ một nhiễm trùng “mô phỏng” bắt chước một trường hợp nhiễm bệnh thật sự.
Bước 2 Thử nghiệm tiền lâm sàng
Sau khi sản xuất, trước khi thử nghiệm trên người, vaccinemới sẽ trải qua quá trình điều tra cẩn thận trong phòng thí nghiệm, sau đó là thử nghiệm trên động vật.
Vaccinetiềm năng sẽ được kiểm tra kỹ lưỡng để đảm bảo độ tinh khiết cần thiết và khả năng kích thích miễn dịch thích hợp. Hiệu quả của việc thêm bất kỳ hệ thống bổ trợ nào cũng sẽ được đánh giá. Các thử nghiệm trên động vật này phải tuân thủ nghiêm ngặt các quy định, hướng dẫn của cơ quan quản lý.
Bước 3 Thử nghiệm lâm sàng
Sau thử nghiệm tiền lâm sàng, vaccinemới được đưa vào thử nghiệm lâm sàng, trực tiếp trên cơ thể con người qua 3 giai đoạn:
* Giai đoạn 1 Thử nghiệm ở một nhóm rất nhỏ, đôi khi chỉ khoảng 5-6 người, giúp loại bỏ các vấn đề an toàn chính và tìm ra liều lượng phù hợp cho bước tiếp theo trong quy trình thử nghiệm.
* Giai đoạn II Tiêm vaccinecho nhiều người hơn, từ 100 đến 200 người, có khi thử nghiệm đến cả 1000 người. Tại thời điểm này, các nhà nghiên cứu muốn xem liệu vaccinecó đáp ứng miễn dịch phù hợp hay không và theo dõi bất kỳ tác dụng phụ nào có thể xảy ra.
* Giai đoạn III Thường có cả chục ngàn tình nguyện viên khỏe mạnh để nhà sản xuất có cơ hội nhận định tốt hơn về hiệu quả cũng như các vấn đề hiếm gặp không xuất hiện trong giai đoạn II, để quyết định cho việc đưa vaccinevào sử dụng đại trà để ngăn ngừa bệnh.
Bước 4 Phê duyệt-chấp thuận
Tất cả thông tin và dữ liệu được thu thập trong quá trình phát triển và thử nghiệm vaccinemới phải được trình cho các cơ quan quản lý có liên quan ở cấp khu vực và cấp quốc gia. Giải trình tất cả các câu hỏi của các nhà quản lý phải được trả lời đầy đủ để đảm bảo tính thống nhất của các tiêu chuẩn.
Bước 5 Theo dõi-hậu đánh giá
Sau khi ra thị trường, vaccinetiếp tục được theo dõi chặt chẽ ở các cấp độ khác nhau để đánh giá tính an toàn và hiệu quả của nó chặt chẽ và thực tế. Việc theo dõi, đánh giá lâu dài, liên tục cũng là một điều kiện do các cơ quan quản lý cập nhật hiệu quả và cho phép sử dụng vaccinerộng rãi hơn so với đánh giá đầu tiên.
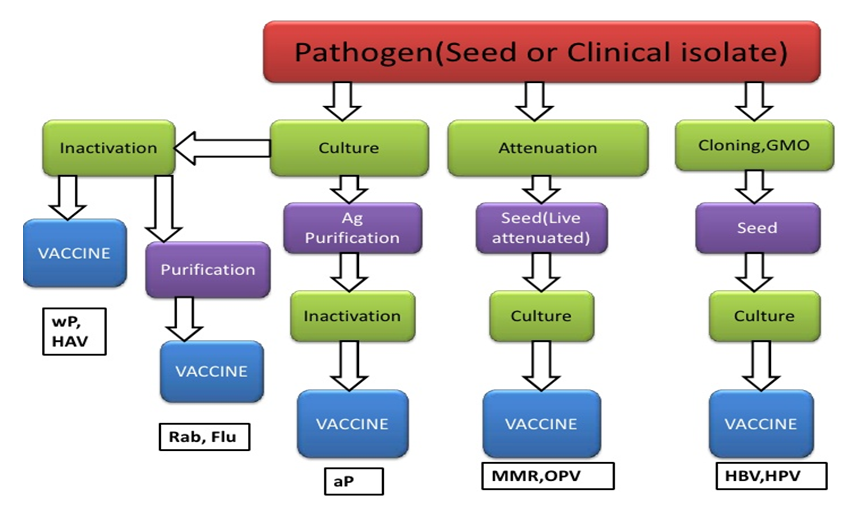
Những vaccine ngừa virus đã được sản xuất
THỜI GIAN NGHIÊN CỨU PHÁT TRIỂN
Vì quá trình sản xuất phức tạp và nhiều trình tự như trên, một vaccine mới từ khi lên kế hoạch thực hiện đến khi được chấp thuận cho sử dụng đại trà cần khá nhiều thời gian.
Theo thống kê y học, với 27 loại vaccine phòng bệnh lây nhiễm đã được chấp thuận dùng đại trà hiện nay, thời gian để phát triển một vaccinelà 27 ± 17,7 năm (4-68 năm), có những vaccine như HIV, sốt rét vẫn chưa hoàn thành [6].
- Rabies – 4 years, 1881-1885 (Schwartz, 2001; Wikipedia)
- Rubella – 7 years, 1962-1969 (Wikipedia)
- Pertussis – 8 years, 1906-1914 (CDC, 2017)
- Measles – 9 years, 1954-1963 (Rice, 2017a)
- Influenza – 14 years, 1931-1945 (WHO, 2009 , p104; Wikipedia)
- Japanese encephalitis – 20 years, 1934-1954 (Artenstein (ed.), 2010, p317; Barrett, 2014, p4)
- Polio – 20 years, 1935-1955 (CDC, 2017; Wikipedia 1; Wikipedia 2; Wikipedia 3)
- Tuberculosis – 21 years, 1900-1921 (Rice, 2017b)
- Mumps – 22 years, 1945-1967 (ProCon, 2017)
- HPV – 23 years, 1983-2006 (WHO, 2009, p116-117; Wikipedia)
- Hepatitis A – 24 years, 1967-1991 (Melnick, 1995; Wikipedia)
- Rotavirus – 26 years, 1980-2006 (Wikipedia 1; Wikipedia 2)
- Smallpox – 26 years, 1770-1796 (Boylston, 2012; Wikipedia)
- Yellow Fever – 27 years, 1912-1939 (Wikipedia; Frierson, 2010)
- Cholera – 30 years, 1854-1884 (WHO, 2009, p104; Wikipedia)
- Chickenpox – 34 years, 1954-1988 (CDC, 2015; Wikipedia)[9]
- Hepatitis B – 38 years, 1943-1981 (CDC, 2017)
- Tick-borne encephalitis – 39 years, 1937-1976 (Wikipedia; WHO, 2016, Slide 5; Baselli, et. al., 2011)
- Diptheria – 40 years, 1883-1923 (WHO, 2009, p106; Rice, 2017c)
- Tetanus – 40 years, 1884-1924 (CDC, 2017)
- Hib disease – 44 years, 1933-1977 (Wikipedia 1; Wikipedia 2)
- Ebola – ~46? years, 1976-2022(?) (Johnson, Lange, Webb, & Murphy, 1977; Pattyn, et. al., 1977; Lupton, et. al., 1980)
- HIV – ~46? years, 1984-2030(?) (Esparza, 2013; Hecht & Jameson, 2011)
- Typhoid – 58 years, 1838-1896 (Wikipedia 1; Wikipedia 2)
- Malaria – ~58? years, 1967-2025(?) (GAVI, 2016; Wikipedia)
- Pneumococcal disease – 66 years, 1911-1977 (CDC, 2017)
- Meningitis – 68 years, 1906-1974 (Flexner & Jobling, 1907; CDC, 2015)
Lịch sử phát triển 27 vaccine đang sử dụng [6]
Hiện nay, với sự tiến bộ của công nghệ gene di truyền, thời gian để phát triển một vaccine phòng bệnh đã giảm xuống rất nhiều, nhưng ít nhất cũng cần khoảng một năm. Ví dụ: Năm 2002-2003 dịch SARS xảy ra, các nhà khoa học phải mất 20 tháng sau mới có vaccine thử nghiệm trên người khi dịch bệnh đã được kiểm soát; Năm 2015 dịch Zika bùng phát, các nhà khoa học cũng mất khoảng 6 tháng để phát triển được vaccine cho virus này.
SẼ SỚM CÓ VACCINE NGỪA COVID-19 ?
Năm ngoái, ngay sau khi nhiều quốc gia thông báo đã phân lập và nuôi cấy thành công Coronavirus 2019-nCoV: Trung Quốc (10/01/2020), Úc (29/01), Pháp (31/01), Nhật (01/02), Việt Nam (07/02)…nhiều viện nghiên cứu, hãng dược phẩm đã nhanh chóng chạy đua sản xuất vaccine cho loại virus nguy hiểm này, với nhiều tuyên bố “có cánh”…
Liên minh đổi mới chống dịch bệnh (Coalition for Epidemic Preparedness Innovations, CEPI), Mỹ, tài trợ cho hai công ty Inovio Pharmaceuticals Inc. San Diego, và Moderna Inc, Massachusetts, thông báo rằng vaccine của họ có thể sẵn sàng tiến hành thử nghiệm tiền lâm sàng trên động vật trong vòng 1 tháng và thử nghiệm lâm sàng trên người trong 3 tháng. Công ty Inovio còn cho biết, nếu thử nghiệm lâm sàng ban đầu (giai đoạn I) trên người thành công thì sẽ thử nghiệm lớn hơn vào cuối năm ngay tại Trung Quốc.
Nhóm nghiên cứu ở ĐH Queensland, Úc, đặt mục tiêu có vaccine thử nghiệm trên người trong 16 tuần nữa.
Ngày 28/1, GS Viên Quốc Dũng, ĐH Hồng Kông, cho biết nhóm nghiên cứu của ông đã sản xuất được vaccinengừa nCoV nhưng cần nhiều tháng để thử nghiệm tiền lâm sàng trên động vật, và ít nhất một năm để thử nghiệm lâm sàng trên người.
Nhóm nghiên cứu của GS Robin Shattock, ĐH St Mary Imperial, Anh, cho biết họ đã tạo ra vaccinevới virus corona trong phòng thí nghiệm. Vaccinenày sẽ được thí nghiệm trên động vật vào ngày 10/02, và nếu thành công đưa vào thí nghiệm lâm sàng vào đầu tháng 6/2020 này.
BÀN VÀ KẾT LUẬN
Về lý thuyết, khi đã phân lập và nuôi cấy thành công mầm bệnh, con người đã qua được bước quan trọng đầu tiên: xác định được kháng nguyên để tạo vaccine tương ứng.
Với sự tiến bộ trong công nghệ gene, đoạn acid nucleic mã hoá cho protein gai S (spike protein) của virus có khả năng kích hoạt hệ miễn dịch trong cơ thể người mà không gây bệnh cho người được tiêm vaccine khiến việc sản xuất nhanh hơn rất nhiều, chỉ cần biết trình tự hệ gen của virus mà không cần thực hiện trên mẫu virus thật. Bà Kate Broderick, dẫn đầu dự án sản xuất vaccine SARS-CoV-2 của Inovio tuyên bố, chỉ 3 giờ sau khi Trung Quốc cung cấp trình tự bộ gene công ty đã có thể thiết kế sản xuất vaccine !
Nhưng trong thực tế, chỉ khoảng 22% vaccine được phát triển được thành công, nghĩa là đến 4,5 nghiên cứu thất bại mới có 1 vaccine khả thi [6], và nhiều mầm bệnh đã được xác định, dày công nghiên cứu, đến nay vẫn chưa phát triển được vaccine phòng bệnh. Điển hình là các bệnh sốt rét, HIV, Ebola…
Theo GS Nguyễn Văn Tuấn, Viện nghiên cứu Garvan, ĐH New South Wale, Úc, hiện nay đã có đến 4 chủng coronavirus sống chung với con người và gây ra cảm cúm mỗi năm, và tương lai có thể chúng ta phải chấp nhận sống chung SARS-CoV-2 như là thành viên thứ 5 của họ coronavirus này.
Do đó, trong khi chờ đợi sự ra đời của vaccine đặc hiệu, cần:
- Nghiêm chỉnh chấp hành các quy định về giãn cách xã hội và cách ly bệnh nhiễm.
- Chủ động áp dụng 5K, các cách thức chung, để phòng ngừa lây nhiễm virus: Vệ sinh cá nhân và môi trường (rửa tay, mặt, súc miệng, lau sạch bàn ghế, đồ dùng cá nhân, gia đình …); Tránh lây nhiễm với khẩu trang, găng tay, kiếng mắt…), Tăng cường sức đề kháng (thực phẩm, vitamin C…), và Thường xuyên cập nhật các hướng dẫn của các cơ quan y tế.
TÀI LIỆU THAM KHẢO
[1] How are new vaccines developed ?https://www.vaccinestoday.eu/stories/how-are-new-vaccines-developed/
[2] How we develop new vaccines
https://www.gsk.com/en-gb/research-and-development/development/how-we-develop-new-vaccines/
[3] Making vaccines: process of vaccine development
[4] Vaccine development
https://www.sciencedirect.com/topics/medicine-and-dentistry/vaccine-development
[5] Vaccine production techniques
https://www.slideshare.net/Drvijayata/vaccine-production-techniques
[6] How long does it take to research and develop a new vaccine?
[7] Coronavirus: Scientists race to develop a vaccine
https://www.bbc.com/news/health-51299735
[8] Chinese scientists race to develop vaccine for nCoV
[9] Scientists race to develop vaccine for coronavirus
http://www.theindependentbd.com/printversion/details/234671
[10] Scientists race to develop vaccine for coronavirus. Experts say it could take over a year
[11] Researchers are racing to make a coronavirus vaccine d
https://www.nytimes.com/2020/01/28/health/coronavirus-vaccine.html
[12] Hồng Kông chế được vaccinevi rút viêm phổi Vũ Hán [13] Trung Quốc bắt đầu phát triển vaccine chống virus Coronahttp://kinhtedothi.vn/trung-quoc-bat-dau-phat-trien-vac-xin-chong-virus-corona-363404.html
[14] Anh đã phát triển vaccinecho virus corona chỉ sau 14 ngày?
[15] Gấp rút phát triển vắcxin ngừa virus corona
https://vnexpress.net/khoa-hoc/gap-rut-phat-trien-vacxin-ngua-virus-corona-4048326.html
[16] Israel bắt tay phát triển vaccinephòng chống virus Corona
[17] Bao nhiêu loại vaccinevà cách điều trị corona đang được nghiên cứu?
[18] GS Nguyễn Văn Tuấn: Ba kịch bản cho dịch bệnh virus Corona
[19] COVID-19 vaccines
https://en.wikipedia.org/wiki/COVID-19_vaccine
A COVID‑19 vaccine is a vaccine intended to provide acquired immunity against severe acute respiratory syndrome coronavirus 2 (SARS‑CoV‑2), the virus that causes coronavirus disease 2019 (COVID‑19). Prior to the COVID‑19 pandemic, an established body of knowledge existed about the structure and function of coronaviruses causing diseases like severe acute respiratory syndrome (SARS) and Middle East respiratory syndrome (MERS). This knowledge accelerated the development of various vaccine technologies during early 2020.[1] On 10 January 2020, the SARS-CoV-2 genetic sequence data was shared through GISAID, and by 19 March, the global pharmaceutical industry announced a major commitment to address COVID-19.[2] The COVID‑19 vaccines are widely credited for their role in reducing the spread, severity, and death caused by COVID-19.[3]
In Phase III trials, several COVID‑19 vaccines have demonstrated efficacy as high as 95% in preventing symptomatic COVID‑19 infections. As of July 2021, 20 vaccines are authorized by at least one national regulatory authority for public use: two RNA vaccines (Pfizer–BioNTech and Moderna), nine conventional inactivated vaccines (BBIBP-CorV, Chinese Academy of Medical Sciences, CoronaVac, Covaxin, CoviVac, COVIran Barakat, Minhai-Kangtai, QazVac, and WIBP-CorV), five viral vector vaccines (Sputnik Light, Sputnik V, Oxford–AstraZeneca, Convidecia, and Janssen), and four protein subunit vaccines (Abdala, EpiVacCorona, Soberana 02, and ZF2001).[4][5]
In total, as of July 2021, 330 vaccine candidates are in various stages of development, with 102 in clinical research, including 30 in Phase I trials, 30 in Phase I-II trials, 25 in Phase III trials, and 8 in Phase IV development.[4]
 Y khoa Diễn đàn Y khoa, y tế sức khoẻ, kiến thức lâm sàng, chẩn đoán và điều trị, phác đồ, diễn đàn y khoa, hệ sinh thái y khoa online, mới nhất và đáng tin cậy.
Y khoa Diễn đàn Y khoa, y tế sức khoẻ, kiến thức lâm sàng, chẩn đoán và điều trị, phác đồ, diễn đàn y khoa, hệ sinh thái y khoa online, mới nhất và đáng tin cậy.




![[Medicalnewstoday] Omicron: Chúng ta biết gì về 'biến thể tàng hình' này? Omicron BA.2 GettyImages1363199780 Header 1024x575 1](https://ykhoa.org/wp-content/uploads/2022/02/Omicron_BA.2_GettyImages1363199780_Header-1024x575-1-310x165.jpg)
![[COVID-19] Trải nghiệm mắc bệnh COVID-19 và vài chia sẻ 273783662 5438275336186793 7547455884400680957 n](https://ykhoa.org/wp-content/uploads/2022/02/273783662_5438275336186793_7547455884400680957_n-310x165.jpg)
![[Medscape] Nhiễm COVID-19 vào cuối thai kỳ liên quan đến các biến chứng ảnh hưởng đến sinh nở ở những phụ nữ chưa được tiêm chủng. tiem vaccine ngua covid 19 cho phu nu mang thai 2.jpeg e1630311032462](https://ykhoa.org/wp-content/uploads/2022/02/tiem-vaccine-ngua-covid-19-cho-phu-nu-mang-thai-2.jpeg-e1630311032462-310x165.jpg)
![[Medicalnewstoday] Triệu chứng khi nhiễm biến thể Omicron Omicron infections testing header 1024x575 4](https://ykhoa.org/wp-content/uploads/2022/02/Omicron-infections-testing-header-1024x575-4-310x165.jpg)
![[Uptodate] Quản lý bệnh nhân Đái tháo đường trong thời kỳ COVID-19 dtd](https://ykhoa.org/wp-content/uploads/2022/02/dtd-310x165.png)
![[COVID-19] "SƯƠNG MÙ NÃO" - DI CHỨNG COVID Y HỌC CHƯA THỂ LÝ GIẢI lims](https://ykhoa.org/wp-content/uploads/2022/02/lims-310x165.jpg)