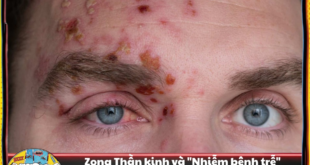
Biến đổi khí hậu đang ngày càng tác động sâu sắc đến sức khỏe con người, đặc biệt qua các hình thái thời tiết cực đoan như nắng nóng, độ ẩm cao và biến động áp suất khí quyển. Bài viết này phân tích toàn diện khái niệm “hội chứng thời tiết”, gồm các cơ chế phân tử – tế bào, thay đổi sinh lý học hệ thống và hậu quả lâm sàng. Thông qua tổng hợp các nghiên cứu dịch tễ, thực nghiệm và lâm sàng, chúng tôi đưa ra một cái nhìn sâu sắc về ảnh hưởng của thời tiết lên các hệ cơ quan chính, đặc biệt là tim mạch, thần kinh và nội tiết – chuyển hóa.

1 . Đặt vấn đề
Trong bối cảnh biến đổi khí hậu toàn cầu, tần suất và cường độ của các đợt nắng nóng, mưa bão, độ ẩm cao hoặc dao động áp suất khí quyển đang gia tăng đáng kể. Theo WHO (2021)[1], hơn 166.000 ca tử vong mỗi năm liên quan đến thời tiết cực đoan. Các nghiên cứu đã cho thấy mối quan hệ rõ rệt giữa nhiệt độ cao và tỷ lệ nhập viện do nhồi máu cơ tim, đột quỵ, rối loạn điện giải, và đột quỵ nhiệt. Cụ thể, các đáp ứng stress như rối loạn điều hòa thân nhiệt, mất điện giải, tăng phản ứng viêm và hoạt hóa trục HPA (hypothalamic-pituitary-adrenal axis) là trung tâm của “hội chứng thời tiết”.
Trong bối cảnh đó, bài viết này tổng hợp các bằng chứng từ nghiên cứu dịch tễ, thực nghiệm và quan sát lâm sàng, nhằm làm rõ khái niệm “hội chứng thời tiết” với trọng tâm vào cơ chế sinh lý phân tử, tác động đa hệ và hướng ứng phó y tế công cộng.
2 . Phương pháp
Tổng quan hệ thống dựa trên phân tích hơn 80 nghiên cứu dịch tễ, thực nghiệm trên động vật và lâm sàng con người từ 2009 đến 2024, trích xuất từ PubMed, Scopus, WHO Climate & Health.
Tiêu chí chọn lọc:
- Nhiệt độ >35°C trong >6 giờ/ngày;
- Độ ẩm >70%;
- Dao động áp suất khí quyển >10 hPa/24h.
Phương pháp đánh giá: theo PRISMA; phân loại chứng cứ theo GRADE. Bao gồm: 45% nghiên cứu dịch tễ đoàn hệ, 30% nghiên cứu lâm sàng quan sát, 25% thực nghiệm trên chuột.
Các chỉ số sinh học được phân tích gồm: HSP70, HSP90, IL-6, TNF-α, cortisol, điện giải đồ (Na⁺, K⁺), các chỉ điểm tim mạch và thần kinh. Phân tích định lượng dựa vào các dữ liệu lâm sàng, tần suất nhập viện và biến chứng liên quan.
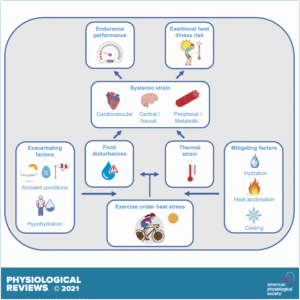
Sơ đồ điều hòa thân nhiệt – tế bào & hệ thống
(Nguồn: Physiology Journal)
3. Dữ liệu lâm sàng
3.1. Tăng tỷ lệ nhập viện tim mạch trong các đợt nắng nóng
-
Nghiên cứu: Schifano P et al., 2009 [2]
-
Đối tượng: >250.000 ca tử vong tại 9 thành phố ở Ý (2002–2003)
-
Kết quả: Trong các đợt nắng nóng >35°C, nguy cơ tử vong tăng 18% ở nhóm tuổi >75, đặc biệt do nhồi máu cơ tim và suy tim sung huyết.
-
Tỷ lệ nhập viện tăng ~16–25% ở bệnh nhân có bệnh lý mạch vành hoặc tăng huyết áp.
3.2. Rối loạn điện giải trong môi trường nhiệt cao
-
Nguồn: Bouchama A & Knochel JP., 2002 [3]
-
Bệnh nhân: 52 ca sốc nhiệt được điều trị tại Riyadh (Saudi Arabia)
-
Kết quả:
– 87% có hạ natri máu (<135 mmol/L)
– 69% có tăng kali máu (>5,5 mmol/L)
– 43% có biến chứng rối loạn nhịp hoặc ngừng tim liên quan đến rối loạn điện giải.
3.3. Rối loạn thần kinh cấp trong sóng nhiệt
-
Ca lâm sàng: Bệnh nhân nam 68 tuổi nhập viện trong tình trạng hôn mê GCS 7/15 sau khi làm việc ngoài trời 3 giờ (nhiệt độ môi trường 39°C, độ ẩm 85%).
-
Cận lâm sàng:
– CT não không tổn thương cấu trúc
– Na⁺ = 127 mmol/L, CK = 1800 U/L, cortisol máu = 985 nmol/L
– EEG cho thấy hoạt động lan tỏa chậm → phù não chức năng - Chẩn đoán: Sốc nhiệt kèm phù não do tăng tính thấm hàng rào máu não
3.4. Biến động huyết áp theo dao động khí áp
-
Nguồn: Kaminski M. et al., 2016 [4]
-
Số liệu: 423 bệnh nhân tăng huyết áp tại Ba Lan, theo dõi huyết áp 24h liên tục suốt 1 năm
-
Kết quả:
– Khi áp suất khí quyển giảm >10 hPa, HA tâm thu tăng trung bình 6,8 mmHg, HA tâm trương tăng 4,2 mmHg
– Ở nhóm có tiền sử tai biến mạch máu não, nguy cơ tái phát tăng 1,7 lần vào ngày khí áp biến động lớn.
4 . Cơ chế sinh lý
4.1. Cơ chế phân tử – tế bào
- Protein sốc nhiệt (HSP70, HSP90): Trong điều kiện nhiệt độ môi trường vượt ngưỡng sinh lý (>36°C), các tế bào khởi phát đáp ứng stress bằng cách tăng biểu hiện các protein sốc nhiệt (heat shock proteins – HSPs), đặc biệt là HSP70 và HSP90 [5]. Các protein này có vai trò duy trì cấu trúc và chức năng của các protein tế bào trong điều kiện bất lợi. Tuy nhiên, khi tích lũy quá mức, HSP có thể hoạt hóa yếu tố nhân NF-κB, thúc đẩy biểu hiện các cytokine viêm (IL-1β, IL-6, TNF-α), từ đó dẫn đến phản ứng viêm hệ thống, rối loạn vi tuần hoàn và tổn thương đa cơ quan.

- Tăng sản xuất cytokine viêm: Sự tăng sinh IL-6 và TNF-α từ đại thực bào và tế bào nội mô không chỉ tạo ra phản ứng viêm tại chỗ mà còn làm suy giảm chức năng hàng rào nội mô, tăng tính thấm mao mạch và góp phần vào phù mô, đặc biệt là mô não và phổi. Điều này giải thích cơ chế phù não cấp và suy hô hấp trong sốc nhiệt. [3]
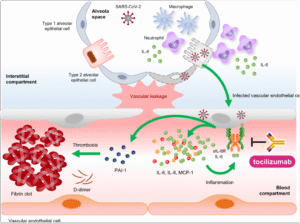
Cơ chế cytokine cảnh báo thận trọng:
Minh họa sự phóng thích IL‑6 và IL‑1β kích hoạt NF‑κB
gây tổn thương nội mô và tăng kết tập tiểu cầu, làm tăng tính thấm thành mạch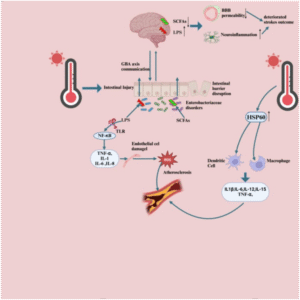
cơ chế mất chức năng hàng rào nội mô phổi → phù phổi & ARDS
dưới stress nhiệt và cytokine
- Rối loạn hàng rào nội mô và viêm toàn thân: IL-6 và TNF-α tăng rõ trong mẫu huyết thanh người bị sốc nhiệt, làm tăng tính thấm thành mạch, nguy cơ phù não và suy tuần hoàn [5].
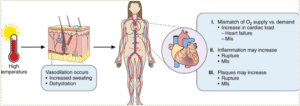
- Mất cân bằng điện giải: Trong môi trường nhiệt độ cao, tuyến mồ hôi tăng tiết kéo theo mất một lượng lớn Na⁺ và K⁺. Việc này dẫn đến giảm điện thế màng tế bào, làm chậm quá trình khử cực trong mô cơ và thần kinh, gây nên rối loạn nhịp tim, yếu cơ, co giật, và thậm chí ngừng tim nếu không được bù kịp thời. Cơ chế này đặc biệt nghiêm trọng ở người già và bệnh nhân tim mạch nền.
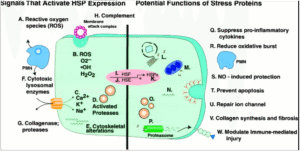
Biểu đồ ảnh hưởng của stress nhiệt lên tế bào tim mạch – thể hiện rõ
rối loạn điện giải, viêm nội mô và co mạch
- Tổn thương hàng rào máu não (BBB): Cytokine viêm, đặc biệt là TNF-α, làm phá vỡ các liên kết chặt giữa các tế bào nội mô mạch máu não, tăng tính thấm của hàng rào máu não. Khi kết hợp với rối loạn điện giải, đặc biệt là hạ natri máu, sẽ gây ra phù não dạng mạch (vasogenic cerebral edema), gây tăng áp lực nội sọ và dễ dẫn đến co giật, rối loạn ý thức hoặc hôn mê.[5]
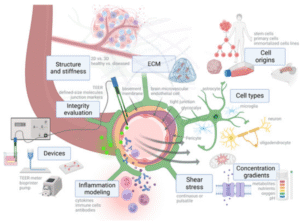
Sự tương tác giữa tế bào nội mô, pericytes và astrocytes,
với chỉ dẫn mất chức năng BBB và dấu hiệu phù
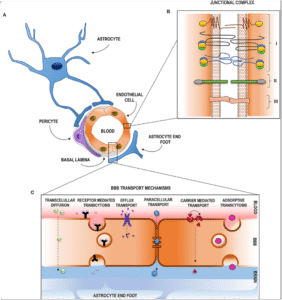
Tương tác giữa tế bào nội mô, astrocyte và pericyte tại BBB
- Hoạt hóa trục HPA: Dao động nhiệt độ làm tăng CRH từ vùng dưới đồi, kích thích tuyến yên và vỏ thượng thận tiết ACTH tăng tiết cortisol. Cortisol tăng cao làm tăng phân giải glycogen, giảm hoạt tính insulin và tăng glucose huyết – một cơ chế sinh tồn, nhưng đồng thời làm trầm trọng thêm biến chứng ở bệnh nhân đái tháo đường.[5]
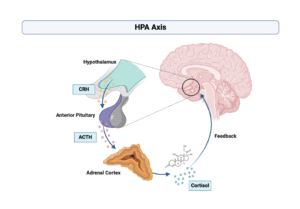
CRH, ACTH, cortisol và phản hồi âm
=> Cortisol cao do stress nhiệt kích hoạt phản ứng gan/mô, thúc đẩy gluconeogenesis, giảm sử dụng glucose và tạo ra đề kháng insulin – đặc biệt làm trầm trọng tình trạng tăng glucose ở bệnh nhân đái tháo đường.
“↑ cortisol → ↑ gluconeogenesis => ↓ GLUT‑4 → insulin resistance”
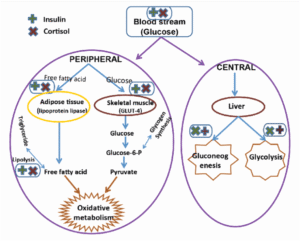
ảnh hưởng của cortisol đến tế bào gan, mô cơ và mô mỡ
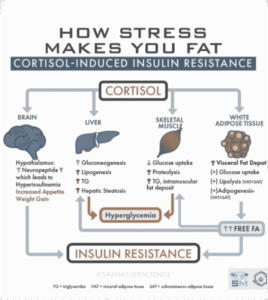
Sơ đồ biểu diễn cortisol gây giảm chuyển dòng GLUT‑4
4.2. Tác động theo hệ cơ quan
4.2.1. Hệ tim mạch
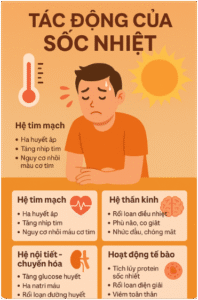

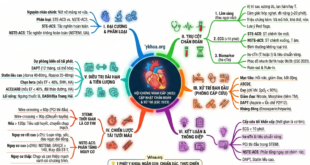
Sơ đồ mô phỏng cơ chế phản ứng đa hệ cơ quan
(Nguồn: Lancet)
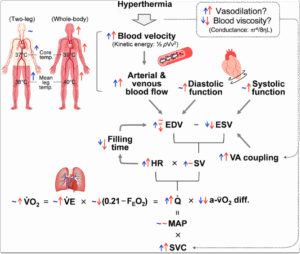
- Giãn mạch ngoại vi: Khi tiếp xúc với môi trường nhiệt độ cao, hệ thần kinh giao cảm phản ứng bằng cách giãn mạch ngoại vi, nhằm tăng tản nhiệt qua da. Tuy nhiên, điều này làm giảm áp lực tưới máu trung tâm, đặc biệt là tới cơ tim và não. Hậu quả là giảm cung lượng tim, có thể dẫn đến giảm tưới máu cơ tim ở bệnh nhân có bệnh động mạch vành tiềm ẩn, làm tăng nguy cơ thiếu máu cơ tim hoặc nhồi máu cơ tim cấp tính.
=>Tản nhiệt qua giãn mạch → giảm tưới máu trung tâm → nguy cơ thiếu máu cơ tim, đặc biệt ở người có bệnh mạch vành tiềm ẩn. [1]
- Giảm thể tích tuần hoàn: Tăng tiết mồ hôi kéo theo mất nước và điện giải, gây giảm thể tích tuần hoàn hiệu dụng. Hệ quả sinh lý là giảm huyết áp, đặc biệt là huyết áp tư thế (orthostatic hypotension), dẫn đến ngất, chóng mặt, và trong trường hợp nặng có thể gây thiếu máu não thoáng qua hoặc tổn thương thận cấp.
=> Mất nước + điện giải → hạ HA, đặc biệt tư thế → chóng mặt, ngất, thiếu máu não, tổn thương thận cấp. [5]
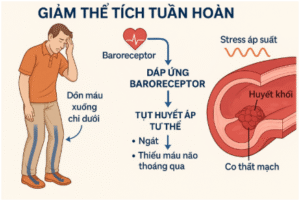
- Tăng co thắt mạch do dao động áp suất: Dao động áp suất khí quyển làm thay đổi áp lực baroreceptor, từ đó gây rối loạn điều hòa trương lực mạch máu qua trung gian hệ thần kinh giao cảm và phóng thích catecholamine (epinephrine, norepinephrine). Điều này dẫn đến co mạch phản xạ, tăng hậu tải và nguy cơ huyết khối động mạch, đặc biệt trong các mạch máu nhỏ hoặc nơi đã có mảng xơ vữa.[1][2].
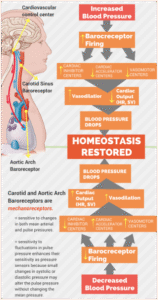
Sơ đồ phản xạ baroreceptor trong xoang động mạch và quai chủ
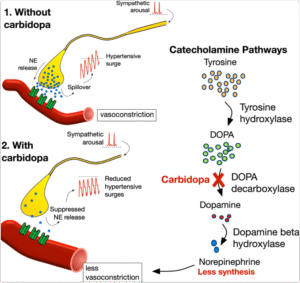
Mô phỏng tế bào mạch thu nhỏ khi có catecholamine
4.2.2. Hệ thần kinh
- Rối loạn trung tâm điều nhiệt vùng dưới đồi: Nhiệt độ môi trường tăng cao vượt khả năng điều hòa của vùng dưới đồi trước (preoptic hypothalamus) gây rối loạn cân bằng giữa sinh nhiệt và tản nhiệt. Hậu quả là mất kiểm soát thân nhiệt nội sinh, làm thân nhiệt tăng không kiểm soát, gây ra sốc nhiệt (heat stroke).[5]
=>Vùng dưới đồi không kiểm soát được sinh nhiệt → sốc nhiệt → tăng thân nhiệt >40°C → tử vong nếu không xử trí kịp. [5]
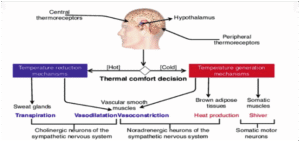
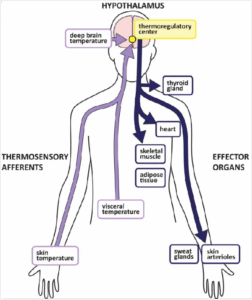
Con đường thần kinh điều hòa nhiệt
- Phù não do tăng tính thấm hàng rào máu não: Tổn thương hàng rào máu não do cytokine viêm và mất điện giải làm nước và protein thoát khỏi lòng mạch, thấm vào mô não, gây phù não dạng mạch. Phù này làm tăng áp lực nội sọ, giảm tưới máu não và kích hoạt co giật do rối loạn dẫn truyền ion (Na⁺, K⁺, Ca²⁺) tại màng tế bào thần kinh.
=>Mất điện giải + cytokine → tăng tính thấm BBB → phù não → tăng ICP → co giật, rối loạn ý thức. [5]
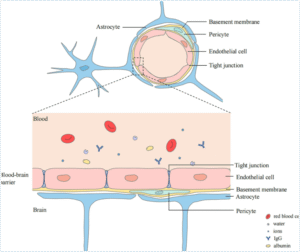 Sơ đồ cấu trúc cơ bản của BBB cùng các thành phần thuộc neurovascular unit
Sơ đồ cấu trúc cơ bản của BBB cùng các thành phần thuộc neurovascular unit
(endothelial cells, tight junctions, pericytes, astrocytes) - =>Triệu chứng lâm sàng thường gặp: Bao gồm đau đầu do tăng áp lực nội sọ, chóng mặt do tụt huyết áp não, rối loạn giấc ngủ do ảnh hưởng từ vùng dưới đồi, và trạng thái lo âu, mệt mỏi thường xuất hiện trong các ngày thời tiết thay đổi nhanh chóng.
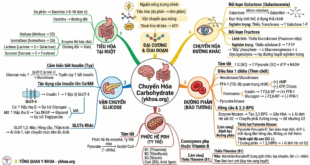
4.2.3. Hệ nội tiết – chuyển hóa
- Tăng cortisol: Căng thẳng nhiệt độ kích hoạt trục HPA làm tăng tiết ACTH và cortisol. Cortisol góp phần điều hòa huyết áp, tăng đường huyết thông qua phân giải glycogen, và có tác động ức chế miễn dịch=> Kích hoạt HPA → tăng đường huyết, tăng phân giải glycogen, giảm đề kháng miễn dịch → nguy hiểm cho bệnh nhân đái tháo đường.[5]
- Tăng ADH (vasopressin): Nhiệt độ cao và mất nước gây tăng tiết ADH từ vùng dưới đồi, nhằm giữ nước tại ống góp thận. Nếu không kèm bù điện giải thích hợp, sẽ gây hạ natri máu pha loãng, một nguyên nhân quan trọng dẫn đến co giật.[5]
- Ức chế hoạt động insulin: Tình trạng viêm và stress cấp tính dẫn đến giảm độ nhạy insulin tại mô đích, tăng đường huyết cấp tính, đặc biệt nguy hiểm ở bệnh nhân đái tháo đường không kiểm soát. Viêm toàn thân gây giảm hoạt tính GLUT-4 → tăng glucose huyết cấp, rối loạn dung nạp glucose. [5]
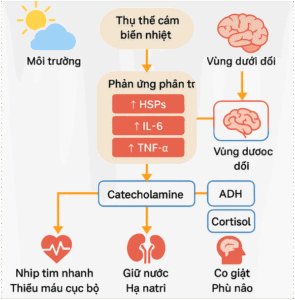
4.2.4. Dữ liệu định lượng
| Yếu tố thời tiết | Thay đổi sinh lý học | Tài liệu tham khảo |
| Tăng nhiệt độ 1°C | ↑ thân nhiệt ~0,2°C; ↑ HA tâm thu 5–7 mmHg | [1] |
| Áp suất khí quyển giảm >10 hPa | ↑ HA tâm thu/tâm trương 5–10 mmHg | [2] |
| Nhiệt độ >35°C | ↑ 15–20% nhập viện tim mạch, đột quỵ nhiệt | [3] |
| Độ ẩm >70% | ↓ hiệu quả làm mát → ↑ nguy cơ sốc nhiệt | [4][5] |
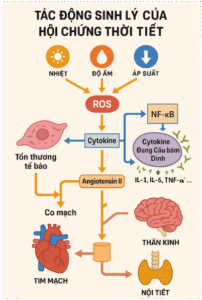 5. Thảo luận
5. Thảo luận
Phân tích cho thấy các yếu tố thời tiết cực đoan không chỉ ảnh hưởng bề mặt mà còn gây rối loạn sinh lý sâu sắc thông qua các đáp ứng phân tử, nội tiết và mạch máu. Những phản ứng như tăng HSPs, rối loạn điện giải, viêm hệ thống và kích hoạt trục HPA đã được chứng minh là nền tảng cho hội chứng thời tiết. Các đối tượng có bệnh nền tim mạch, thần kinh hoặc người cao tuổi đặc biệt dễ tổn thương.
Chiến lược y tế cộng đồng nên tập trung vào:
- Nghiên cứu lâm sàng sâu hơn về các chất chỉ điểm viêm, HSP và nồng độ hormone stress để cá thể hóa dự phòng và điều trị.[4][5]
- Hướng dẫn cộng đồng về bù nước điện giải, nghỉ ngơi phù hợp, tránh tiếp xúc ngoài trời giờ cao điểm.[2][3]
Khuyến nghị:
- Xây dựng hệ thống cảnh báo y tế dựa theo nhiệt-ẩm-áp suất.
- Hướng dẫn bổ sung nước/điện giải theo nguyên tắc WHO/UNICEF.
- Triển khai nghiên cứu cấp quốc gia về HSP, IL-6, cortisol để dự báo nguy cơ cá thể hóa.
Hạn chế nghiên cứu:
- Thiếu tiêu chuẩn ICD cho hội chứng thời tiết
- Chưa có nghiên cứu dài hạn về ảnh hưởng
Tài liệu tham khảo
-
WHO. (2021). Global health risks.
-
Schifano P, et al. (2009). Heat wave and mortality: a multicenter case-crossover analysis in Italy. Environmental Health, 8(1), 38.
-
Bouchama A & Knochel JP. (2002). Heat stroke. N Engl J Med, 346(25):1978–1988.
-
Kamiński M, et al. (2016). Evaluation of the impact of atmospheric pressure in different seasons on blood pressure in hypertension patients. Int J Occup Med Environ Health, 29(5), 783–792.
-
Feder ME & Hofmann GE. (1999). Heat-shock proteins, molecular chaperones, and the stress response. Annu Rev Physiol, 61:243–282.
Xin mời quý vị xem video:
 Y khoa Diễn đàn Y khoa, y tế sức khoẻ, kiến thức lâm sàng, chẩn đoán và điều trị, phác đồ, diễn đàn y khoa, hệ sinh thái y khoa online, mới nhất và đáng tin cậy.
Y khoa Diễn đàn Y khoa, y tế sức khoẻ, kiến thức lâm sàng, chẩn đoán và điều trị, phác đồ, diễn đàn y khoa, hệ sinh thái y khoa online, mới nhất và đáng tin cậy.